
nCounter®
Tumor Signaling 360™ Panel
みなさまの 研究の一助に
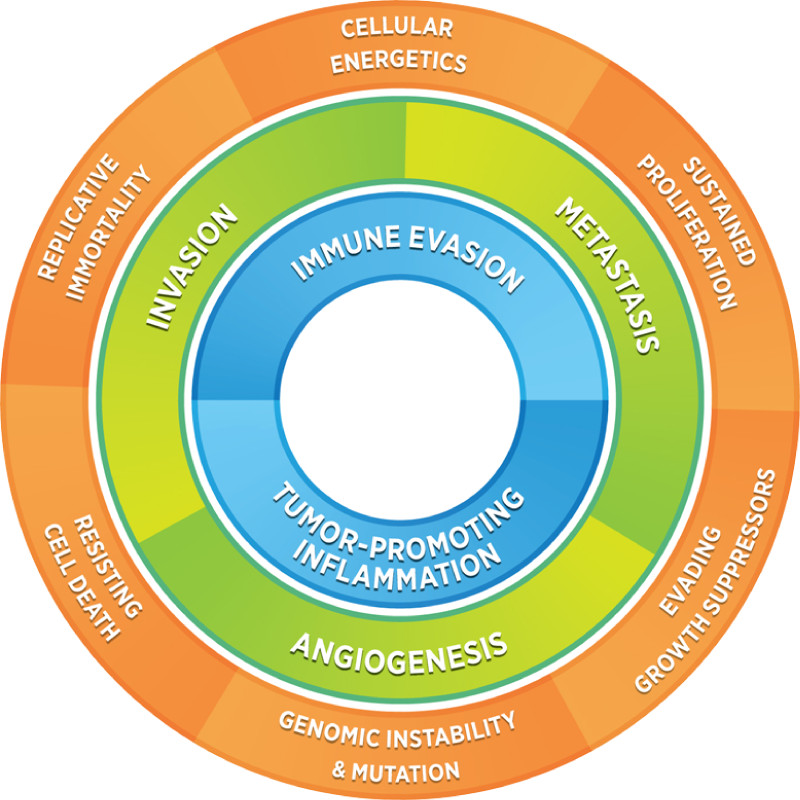
腫瘍シグナリングをターゲットとする治療法の進化に伴い、腫瘍細胞と組織環境の相互作用に対して理解を深めるだけではなく、腫瘍シグナリングに対しても理解を深めることが必要になります。Tumor Signaling 360 Panelは、この用途にまさに適した製品であり、包括的でありながら、ターゲットとする治療法の開発に対応する目的のシグナリングパスウェイにフォーカスした、より高度な腫瘍プロファイリングを実現します。nCounter Tumor Signaling 360 Panelは、腫瘍発生、転移、炎症に関与する多数の遺伝子をカバーし、がんにおける機能不全の細胞のシグナリングに重点を置いた、腫瘍、微小環境、免疫応答の生物学全体ビューを提供します。
- 腫瘍生物学、免疫回避、微小環境リモデリングに関与する40以上のパスウェイをプロファイル
- 新たな治療法のためのターゲットを同定
- ターゲットとする治療の作用機序を把握
- 腫瘍炎症シグネチャーにより、抗腫瘍免疫応答の範囲を判定
- 14の異なる免疫細胞タイプの存在と相対的存在量を定量
NanoStringの360 Series Panel Collectionは、がん研究に対するシステムバイオロジーのアプローチに基づいており、腫瘍、微小環境、免疫応答の生物学に関与する高度にキュレーションされたコンテンツを1つの総括的アッセイにまとめることで、360度ビューの遺伝子発現情報を提供します。各パネルには、末梢性抑制の適応免疫応答の測定が可能で、チェックポイント阻害剤への応答に関連することが示されている、18遺伝子腫瘍炎症シグネチャー(TIS)が含まれています。

製品情報
腫瘍炎症シグネチャーには、PD-1/PD-L1阻害剤への応答に関連することが知られている18の機能的遺伝子が含まれています

免疫生物学の4つの領域(抗原提示に関連するIFN-ү応答遺伝子、ケモカイン発現、細胞障害活性、適応免疫耐性遺伝子)が含まれています
腫瘍炎症遺伝子発現シグネチャーにより、宿主の免疫微小環境の複雑な生物学が示されます。
View publication and video.
- Ayers, Mark, et al. “IFN-y-related mRNA profile predicts clinical response to PD-1 blockade.” The Journal of Clinical Investigation 127.8 (2017).
プラットフォームの仕様(*Prosigna®乳がん予後遺伝子シグネチャーアッセイ(1)には適用されません)
360シリーズ製品の比較
各360 Panelに対応する十分にアノテーションされた遺伝子リストを、Excel形式で提供します。以下の表では、腫瘍、微小環境、免疫応答について、360 PanelとPanCancer Panels Collectionのバイオロジーカバレッジを比較しています。
関連リソース
論文
Assessing Longitudinal Treatment Efficacies and Alterations in Molecular Markers Associated with Glutamatergic Signaling and Immune Checkpoint Inhibitors in a Spontaneous Melanoma Mouse Model
Previous work done by our laboratory described the use of an immunocompetent spontaneous melanoma-prone mouse model, TGS (TG-3/SKH-1), to evaluate treatment outcomes using inhibitors of glutamatergic signaling and immune checkpoint for 18 weeks. We showed a significant therapeutic efficacy with a notable sex-biased response in male mice.
Spatial transcriptomics reveals discrete tumour microenvironments and autocrine loops within ovarian cancer subclones
High-grade serous ovarian carcinoma (HGSOC) is genetically unstable and characterised by the presence of subclones with distinct genotypes. Intratumoural heterogeneity is linked to recurrence, chemotherapy resistance, and poor prognosis.
Spatially Segregated Macrophage Populations Predict Distinct Outcomes In Colon Cancer
Tumor-associated macrophages are transcriptionally heterogeneous, but the spatial distribution and cell interactions that shape macrophage tissue roles remain poorly characterized. Here, we spatially resolve five distinct human macrophage populations in normal and malignant human breast and colon tissue and reveal their cellular associations.



